TEMA BROJA
Miloslav Rajković
Periodni sistem elemenata
Trenutak savršene simetrije

Dmitrij Ivanovič Mendeljejev |
Navršilo se više od jednog i po veka od kada je ruski naučnik Dmitrij Ivanovič Mendeljejev (Дмитрий Иванович Менделеев), profesor Tehničkog instituta Univerziteta u Sankt Peterburgu, u Žurnalu Ruskog fizičko-hemijskog društva (1, 60–77, 1869, p. 70) objavio svoj rad o periodnom zakonu i periodnom sistemu elemenata Соотношение своих свойств с атомным весом элементов (Однос између своjстава и атомских тежина елемената), s tabelarnim prikazom.
Kada se pomene periodni sistem, ime naučnika Mendeljejeva je prva asocijacija. Odmah zatim i druga, ili gotovo istovremeno, da se može videti na zidu hemijske laboratorije svake škole u svetu. Naravno, to odavno nije izvorna tabela slavnog ruskog hemičara, ali koja god verzija bila u pitanju, prožima je početna ideja. Uvek ćemo tabelu hemijskih elemenata zvati njegovim imenom.
O 17. februaru (po julijanskom kalendaru) 1. martu 1869. u hemiji, u Americi je nedavno napisana i jedna doktorska disertacija. Toga dana se dogodilo nešto krupno što je otvorilo nova obzorja u nauci. Pišući svoj glasoviti udžbenik Osnovi hemije, Mendeljejev se pozabavio i idejom klasifikacije dotad poznatih elemenata, otprilike polovinom svih danas poznatih, i podacima koje imao o njima. Napisao je po jednu karticu za svaki od njih i pokušao da ih složi po nekom logičnom redu, za početak po rastućoj atomskoj masi.
Mendeljejevljev san
Dr Tamara R. Todorović, sa Katedre za opštu i neorgansku hemiju Hemijskog fakulteta u Beogradu, prenosi nam o tome sačuvanu akademsku legendu: “Mendeljejev je bio strastveni igrač pasijansa pa je na kartama zapisao simbole elemenata. Slažući karte primetio je da se neki elementi sa sličnim osobinama periodično ponavljaju. Tri dana je kombinovao karte i bezuspešno pokušavao da ih uklopi. Premoren, zaspao je za radnim stolom i u snu ‘video’ na koji način treba poređati elemente. Kada se probudio, svoju viziju je skicirao na parčetu papira, a kasnije objavio”.
Taj autograf periodnog sistema sa datumom 17. februar 1869, od koga se računa era moderne hemije, danas ima i neprocenjivu muzejsku vrednost. Našao je mesto u mnogim udžbenicima hemije i nebrojano puta objavljivan. Prvi put je predstavljen u Ruskom hemijskom društvu. Nije to učinio sam Mendeljejev, zbog bolesti, već njegov kolega Nikolaj Menšutkin. Apstrakt Mendeljevljevog rada, štampanog u martovskom broju Žurnala, objavljen je iste godine u nemačkom časopisu Zeitschrift für Chemie, 1869, 12, 405, a ubrzo preveden na engleski. Ključna rečenica u Mendeljejevljevoj formulaciji bila je: “Elementi poređani po rastućim atomskim masama pokazuju jasnu periodičnost svojstava”.
Čitavih 130 godina kasnije, ovaj san je inspirisao Pola Streterna (Paul Strathern), škotsko-irskog akademika, pisca popularnih knjiga o svetu nauke, autora TV serije The Big Idea: Scientists Who Changed the World, da napiše Mendeleyev's Dream: The Quest for the Elements (2000), knjigu koja je doživela nekoliko izdanja i prevedena na više od dvadeset jezika, a nedavno i The Periodic Table (2015). Mendeljejevljev san je čudesna, donkihotska, slikovita povest o čovekovim pregnućima da otkrije temeljna načela hemije, koja u ovom delu dosežu svoj vrhunac u snoviđenju Periodne tablice. Tablice koja će iz osnova promenti naše razumevanje sveta.

Original tabela |
Često možemo pročitati zapažanje kako je od Prvog svetskog hemijskog kongresa u Karslsrueu, 1860, do otkrića Periodnog sistema bilo potrebno manje od jedne decenije. Pri tom, prof. Tamara Todorović naglašava važnost podatka da su na tom skupu učestvovali najeminentniji hemičari i fizičari toga doba, kao što su: Faradej, Bunzen, Stanislao Kanizaro (Canizzaro), Lotar Majer, sam Mendeljejev, koji je tek bio doktorand. Bio je u društvu istaknutog ruskog hemičara i kompozitora Aleksandra Borodina. Ali da bi se stiglo do tog kongresa, koji je bio posvećen tako krucijalnim pitanjima, kao što su: atomska težina, hemijski simboli i hemijske formule, i potom uloge jednog ljudskog sna u rađanju moderne hemije, koji nije bio tek običan san već san-vizija, pomalo i proročki, moralo je da prođe više od dva milenijuma.
Deset elemenata je bilo poznato još drevnim društvima i civilizacijama, od paleolita do grčke antike: bakar, sumpor, ugljenik, zlato, srebro, gvožđe, kalaj, antimon, živa i olovo. Pojedini od ovih elemenata su obeležili čitava razdoblja, o čemu govore sami nazivi: bakarno, gvozdeno i bronzano doba ili zlatno doba u mitološkim pričama, brojni artefakti nađeni prilikom arheoloških iskopavanja. Prošlo je potom više od hiljadu godina dok je pronađen arsen, pa još četiri veka da bude otkriven fosfor 1669, i da se u tom istom veku shvati da pojam element iz alhemije nije pogodan za naučno objašnjenje raznovrsnosti osobina supstanci i njihovih reakcija. Već je Etjen de Klav (Etinne de Clave) svojom definicijom elemenata kao najjednostavnijih supstanci od čijih su mešavina sastavljena jedinjenja i čija se jedinjenja mogu ponovo razložiti na te iste supstance (1641) nagovestio kraj traganju za “kamenom mudrosti” , a Robert Bojl (Boyl) kritikom njenih nedostataka u radu The Sceptical Chymist (Sumnjičavi hemičar, 1661) srednjovekovnu alhemiju poslao u istoriju. Smatrao je da pod pojmom hemijskog elementa treba podrazumevati supstance koje nisu nastale iz supstanci ili jedni iz drugih, već čine osnovne sastojke iz kojih se sastoje mešane supstance.
Počeci moderne hemije
Nastanak savremene hemije i moderne nauke uopšte, kaže dr Aleksandar Dekanski, naučni savetnik Centra za elektrohemiju u Institutu za hemiju, tehnologiju i metalrugiju Univerziteta u Beogradu - započeo je u trenutku kada je napušteno alhemičarsko mistično tumačenje prirode elemenata i prihvaćeno da se naučno znanje može zasnivati samo na eksperimentisanju i iskustvu. Bojl и Lavoazje (Antoine-Laurent de Lavoisier) bili su prvi koji su tvrdili da se osobine elemenata mogu definisati samo na osnovu iskustvenih opažanja, odbacujući ulogu apstraktnih elemenata.
Muke sa imenom
Imena svih novih elemenata treba da imaju završetak koji odražava i sledi istorijsku i hemijsku konzistentnost i tradiciju - kaže Aleksandar Dekanski. - Tako se sa “-ium” završavaju imena elemenata iz grupe 1-16, sa “ine” iz grupe 17 i sa “on” elementi grupe 18. Na kraju, imena novih hemijskih elemenata na engleskom jeziku moraju da dozvoljavaju jednostavno i ispravno prevođenje na druge jezike. Pre nego što se nova imena odobre, važno je da se dobro pregledaju da li se uklapaju na svim različitim jezicima. Razlog je vrlo jednostavan: da bi se izbegle nedoumice i loši prevodi. Jer postoji mogućnost da se njihovo ime u nekom od jezika podudara sa nekim oblikom postojeće reči ili da je ime gramatički teško standardizovati.
Tajna plutonijuma
Plutonijum je otkriven 1941. u SAD tokom rada na atomskoj bombi, a otkri’e objavljeno 1945. Naučnicima je bilo zabranjeno da za element 94 koriste ime plutonijum, jer je svaki sastojak bombe bila stroga tajna. Zato su taj novi element nazivali bakar, a ako je bilo potrebno da koriste bakar, njega su nazivali „tako mi boga bakar” (honest-to-God copper). Siborg kao njegov pronalazač, kaže A. Dekanski, imao je u to vreme pravo da elementu koji je otkrio da ime i simbol. Po ugledu na godinu ranije otkriven neptunijum, odlučio je da novi element nazove po najmanjoj planeti sunčevog sistema Plutonu, plutonijum. Logično je bilo da simbol bude Pl, ali se Siborg odlučio za Pu. Tajna zašto je tako postupio otkrivena je tek posle njegove smrti 1999, u članku objavljenom u časopisu Los Alamos Science, 17, 2000). Po rečima njegovih kolega u pitanju je bila šala. „Možda i ne sasvim obična”, primećuje naš sagovornik. „Simbol Pu se na engleskom izgovara pi-ju, kao što deca uzviknu kada vide i pomirišu nešto ružno i smrdljivo – Pee- Yoo! Da li je Siborg tako želeo da skriveno iskaže svoj stav što je atomska bomba bačena na Japan? |
Kao što među Leonardovim brojnim anatomskim crtežima treba tražiti začetke neuhvatljivog Monalizinog osmeha, tako u važnim otkrićima s početka XIX veka i prvim pokušajima klasifikacije elemenata treba videti niz koraka koji su doveli do konačnog ustanovljenja periodnog sistema. Otkriće periodnog sistema bio je dug proces, sličan onim procesima dugog trajanja u istoriji, koji je trajao decenijama i u koji je bilo uključeno mnogo ljudi. Naši sagovornici vele da su to u početku manje-više bili laici, da bi se, kao što zapaža Dekanski, “tek poslednjih sedam godina problemu posvetili profesionalni, školovani hemičari”. Taj niz počinje sa Bojlom i Lavoazjeom, a slede ih: Benjamin Rihter i Gotfrid Fišer, Džon Dalton, Gej-Lisak i Aleksandar fon Humbolt, Amadeo Avogadro, Volfgang Deberajner, Vilijam Praut i Leopold Gmeling, Emil B. de Šankurtua i Džon Njulends, Vilijam Odling, Danac Gustavus Hinris, Italijan Stanislao Kanicaro, Lotar Majer.
Kada govorimo o istoriji nastanka periodnog sistema, moramo imati u vidu nekoliko važnih otkrića početkom XIX veka, kao što su ekvivalnetne težine (Rihter/Fišer) 1802, Zakon stalnih zapreminskih masa (Gej-Lisak, 1809), Daltonova atomska teorija 1810, Avogadrova hipoteza 1811, relativne atomske mase (Bercelijus 1826). Lavoazje je 1789. objavio prvi spisak od 33 elementa, na kome su se našli i svetlost (lumiére) i toplota (calorique). Blagodareći brzom razvoju tehnika separacije i analize, u naredne dve decenije otkriveno je 18 novih elemenata. A onda na scenu stupaju prave preteče modernog periodnog sistema.
Džon Dalton, učitelj iz Mančestera, napravio je prvu tabelu sa atomskim težinama koja je imala samo šest elemenata. Deberajner je razvrstao elemente u pet trijada sa po tri elementa: u prvoj grupi su bili elementi koji stvaraju soli (hlor, brom, jod), u drugoj baze, u trećoj baze, četvrtoj kiseline i u petoj gvožđe, kobalt i nikl (metali). “Bio je to prvi nagoveštaj budućih otkrića koja će biti krunisana radovima Mendeljejeva i Lotara Majera”, kaže dr Dekanski.
Jedan pokušaj je učinio škotski hemičar Parut, a Leopold Gmelin je 1843. sve elemente rasporedio u obliku latinskog slova V.
Kongres u Karlsrueu 1860. bio je prekretnica u čitavom procesu. “Na toj prvoj, sada već čuvenoj međunarodnoj konferenciji, hemičara Stanislao Kanicaro (Cannizzaro) je oživeo Avogradovu hipotezu da jednaka zapremina gasova ( pod istim uslovima temperature i pritiska) sadrži jednak broj molekula i na osnovu nje pouzdano i precizno prikazao određene atomske težine poznatih elemenata, i stekli su se preduslovi za razmišljanja o odnosima između ustanovljenih atomskih težina i osobina elemenata. To je dovelo da, u roku od jedne decenije, savremeni periodni sistem bude otkriven”, naglašava dr Dekanski.
Prvi veliki korak je učinio Šankurtua (Émile Béguyer de Chancourtois) kada je u časopisu Francuske akademijenauka Comptes Rendus publikovao prvi trodimenzionalni periodni sistem. On je raspodelio elemente duž spirale opisane oko metalnog cilindra. Izdavač je smatrao da je ilustracija nebitna, pa je nije štampao uz tekst, što je oduzelo vizuelnu vrednost sistemu. Rad je ostao nezapažen (ali ne, kako će se ispostaviti i od Mendeljejeva), a razočarani de Šankurtoa je izgubio interes za svoju ideju.
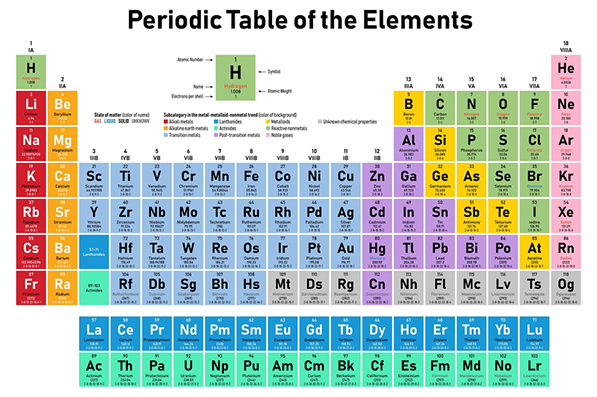
Tabela danas |
Godinu kasnije, 1863, Englez Džon Njulends (Newlands) je najpre podelio elemente u sedam grupa istražujući brojčanu zavisnost njihovih atomskih težina. On je usavršavao svoju tabelu i u Londonskom hemijskom društvu (London Chemical Society), objavio svoj “Zakon oktava” i prikazao tabelu sa 62 elementa podeljenih u osam grupa. Prvi je predvideo postojanje nepoznatih elemenata na osnovu osobina koje se periodično ponavljaju. Ali kako nije imao formalno obrazovanje a ni akademski status, članovi Društva su odbili da publikuju njegov rad. Članak je objavio u časopisu Chemical News jednog privatnog izdavača. Kasnije je njegov doprinos razvoju periodnog sistema bio priznat.
Ugledni i cenjeni naučnik i hemičar Odling (prisustvovao je konferenciji u Karlsrueu), jedan od najvećih zagovornika Kanicarovog pristupa hemiji, objavio je 1864. godine tabelu sa 57 elemenata u kojoj su prvi put izdvojeni prelazni elementi. Ali, kako kaže Dekanski, on sebe nije doživljavao kao “glavnog protagonistu priče o otkrivanju i sistematizaciji elemenata” pa se posvetio fundamentalnoj nauci, smatrajući ovo običnom klasifikacijom.
Gustavus Hinris (Hinrichs) se u definisanju periodnog sistema oslanjao na astronomiju, spektroskopiju i mineralogiju, pa i na numerologiju. Svoje ideje o periodnom sistemu je prvi put izneo 1855, a potpuno definisan sistem u knjizi Atomehanika ili hemija mehanike panatoma 1857, u SAD, gde je radio na Univerzitetu Ajova. Osnovu njegove teorije čine panatomi, od kojih su elementi sačinjeni. Njegove “kontroverzne ideje” učinile su da zapažanja koja je izneo ne budu ozbiljno razmatrana. Ipak, vredno je što je bakar, zlato i srebro smestio u istu grupu, što je propustio da ustanovi i sam Mendeljejev.
Preduslov važnih otkrića
Poslednji u ovom nizu, nemački hemičar Lotar Majer, sačinio je savremeni periodni sistem, sličan Mendeljejevljevom, ali je svoju konačnu verziju iz 1868. objavio posle 27 godina. “Ostaje pod sumnjom da li je ta tabela zaista tako izgledala kada je nastala ili je u međuvremenu dodatno korigovana?”, pita se A. Dekanski, uz napomenu da je izgled Majerove tabele “konzistentnije i precizniji” od one koju je objavio Mendeljejev, uključujući i ispravno postavljanje žive sa kadmijum, kalaja sa olovom i talijuma sa borom, što Mendeljejev nije učinio ni u jednom slučaju.
Zašto je Lotar Majer ostao po strani iako je on dao svoju verziju periodnog sistema, skoro identičnu Mendeljejevljevoj? “Upravo zbog toga što je Mendeljejev bio dovoljno hrabar da stane iza svog dela i da kaže: ovde je mesto za element koji nije otkriven, i opet, ovde je mesto za element koji još nije otkriven. Korigovao je atomske težine i položaje nekih poznatih elemenata, na primer, telura i joda. Majer je objasnio samo fizička svojstva elemenata, za razliku od Mendeljejeva koji je obratio pažnju na njihova hemijska svojstva. Obojica su dobili priznanje za svoj rad, Dejvijevu medalju, ali je Mendeljejevu pripala zaslužena slava, pa je i danas periodni sistem poznat pod njegovim imenom”, kaže prof. Marija Todorović.
Otkrića (i sinteze veštačkih) elemenata koje su usledile narednih godina (galijum, skandijum, germanijum, i decenija, sve do naših dana, u potpunosti su potvrdile pretpostavke koje je Mendeljejev izneo u svom radu o periodnom zakonu i periodnom sistemu.
Ispostavilo se da je njegovo ustanovljenje, kaže Dekanski, bio preduslov mnogim važnim, možda i najvažnijim, naučnim otkrićima u poslednjih vek i po, kao što su otkriće radioaktivnosti (1886), plemenitih gasova (čitava grupa periodnog sistema) 1894, prirode radioaktivnosti (Raderford 1903), strukture atoma (Nils Bor 1913), neutrina (Čedvik 1932), aktinoida i lantanoida (Siborg i saradnici 1951).
Glen Siborg, američki naučnik švedskog porekla, proveo je veći deo radnog veka u Lorenc Berkli nacionalnoj laboratoriji univerziteta Kalifornija, tokom četvrte i pete decenije XX veka bio je glavni ili veoma značajan pronalazač u timovima koji su otkrili i istraživali deset transuranijumskih elemenata: plutonijum (element 93), americijum (95), kirijum (96), berklijum (97), kalifornijum (98), ajnštajnijum (99), fermijum (100), mendeljevijum (101), nobelijum (102) i siborgijum (106). Bio je savetnik za nukelarnu politiku deset američkih predsednika, od Trumana do Klintona. To je bio razloga da su američki naučnici izvršili snažan pritisak na IUPAC da se se elementu 106 da ime siborgijum još za njegova života.

Dr Dekanski |
Periodna tabela hemijskih elemenata je od Mendeljeva nekoliko puta menjala izgled. “Prva izmena je usledila nakon otkrića rendgenskih zraka”, priča prof. Todorović. “Henri Mozli, engleski naučnik, eksperimentisao je sa novootkrivenim zracima, pa tako danas znamo da su to rendgenski ili X-zraci. Mozli je napravio niz anoda od različitih elemenata, uglavnom metala, i bombardovao ih ubrzanim elektronima pri čemu se emitovalo karakteristično elektromagnetsko zračenje, koje je zavisilo samo od prirode elementa od koga je napravljena anoda. Mozli je beležio spektre tog zračenja i zaključio da frekvencija, odnosno talasna dužina tog zračenja raste ako se u Periodnom sistemu ide od jednog elementa do drugog. Izvršio je određene ekstrapolacije i svakom elementu dao redni broj. Ispostavilo se da je to tačno uradio i da redni broj zapravo predstavlja broj protona u jezgru i elektrona u omotaču. Zahvaljujući Mozliju mi danas znamo da su fizička i hemijska svojstva elemenata periodična funkcija njegovog rednog broja a ne relativne atomske mase. Druga promena je usledila posle otkrića kvantne hemije, a najveća kada je Glen Siborg lantanoide i aktinoide izdvojio u posebne redove. Najnovija promena dogodila se pre četiri godine, kada je tabela periodnog sistema popunjena sa poslednja četiri elementa čija imena su: 113 nihonijum (Nh), 115 moskovijum (Ms), 117 tenesin (Ts) i 118 oganeson (Og).“
Usvojena imena su morala biti u skladu sa smernicama IUPAC za imenovanje elemenata, koje su nedavno korigovane i dozvoljavaju da se novootkriveni elementi mogu nazvati po; mitološkoj ličnosti ili pojmu, uključujući astronomske objekte); mineralnim ili sličnim supstancama; mestu ili geogarfskoj oblasti, osobini elementa ili imenu naučnika. Učinjen je još jedan presedan, pa je poslednji element u periodnom sistemu, oganeson dobio ime po još živom ruskom naučniku Juriju Oganesijanu.
Najdragocenija tabela
Svi elementi od 95. nadalje su, kaže dr Dekanski, sintetički, od 100. nepoznatog agregatnog stanja, a od 109 (osim elementa 112 kopernicijum) i nepoznatih hemijskih svojstva. Od 94 prirodna elementa,11 se mogu pronaći samo u lancima raspadanja primordijalnih elemenata. Većina transuranijumskih elemenata ima kratak vek raspadanja, čak kraći od jedne sekunde, a sintetisani su u količinama od samo nekoliko atoma, pa im nije moguće odrediti hemijske osobine, štaviše ni agregatno stanje.
Aktuelni periodni sitem sadrži 118 elemenata, a poslednja četiri sintetisana popunila su njegov sedmi red. Pre nego što su ta četiri elementa zauzela svoja mesta, tadašnji predsednik hemijske sekcije Međunarodne unije čiste i primenjene hemije Jan Ridijk (Reedijk) sa Univerziteta u Lajdenu (Nizozemska) nestrpljenje naučnika je izrazio rečima: “Hemičari jedva čekaju da vide najdragoceniju tabelu čiji je sedmi red popunjen”, a nobelovac Rjođi Nojori da to “za naučnike ima veću vrednost od olimpijske medalje”. Kada se to konačno dogodilo, dr Piter Voters, sa Kembridža, mogao je konačno da uživa u lepoti simetrije: Periodna tabela je sada potpuno simetrična. Otkad postoji, ovo je njeno najsavršenije izdanje, verovatno i jedini trenutak kada izgleda kompletirano. Čim se otkrije novi element, on će biti usamljen u osmom redu.
Profesor Tamara Todorović je jedno svoje predavanje prošle godine naslovila: Periodni sistem elemenata - od skice do remek-dela. Leonardo da Vinči je do poslednjeg daha usavršavao svoje remek-delo - Mona Lizu, Đokondin osmeh. Hemičari su, tragom Mendeljejevljevih predviđanja, njegovu periodnu tabelu dopunjavali i usavršavali vek i po, do njenog najsavršenijeg izgleda. Umesto zaključka, ona citira Džejmsa Emslija (James Emsley, Elements), pisca naučno-popularnih knjiga, za koga je Periodni sistem jedno od najvećih dostignuća nauke uopšte, koji svoju tvrdnju potkrepljuje nepobitnim zaključkom: Ako jednog dana uspemo da stupimo u kontakt sa nekom vanzemaljskom inteligentnom kulturom, možemo biti sigurni da će zajedničko za obe biti uređen sistem elemenata koji će biti odmah prepoznat od oba inteligentna oblika života.
U ovim rečima prepoznajemo davnašnju misao Karla Sagana: Svi smo sazdani od zvezdane prašine.
Hemičari nastavljaju da tragaju za elementom 119, i svim ostalim iz osmog reda. Koja je najveća moguća atomska težina jednog elementa?, pita se Aleksandar Dekanski. U tome, ipak, ne možemo ići u beskonačno, odgovara prof. Marija Todorović.
Miloslav Rajković
Kompletni tekstove sa slikama i prilozima potražite u magazinu
"PLANETA" - štampano izdanje ili u ON LINE prodaji Elektronskog izdanja
"Novinarnica"
|

